Решебник по химии 9 класс Габриелян | Страница 12
Страница 12
Используйте дополнительную информацию
11. Растворимость веществ в воде зависит от температуры. Твёрдые вещества, как правило, при нагревании растворяются лучше, газообразные — наоборот. Данные о зависимости растворимости от температуры можно найти в справочниках. Например, для хлорида калия справочные данные таковы:
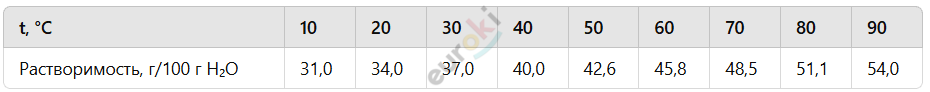
Постройте график данной зависимости в координатах растворимость — температура, воспользовавшись офисным приложением Excel.
Вот график зависимости растворимости хлорида калия (KCl) от температуры. Как видно, с повышением температуры растворимость увеличивается почти линейно: при 10 °C — около 31 г, а при 90 °C — уже 54 г на 100 г воды.
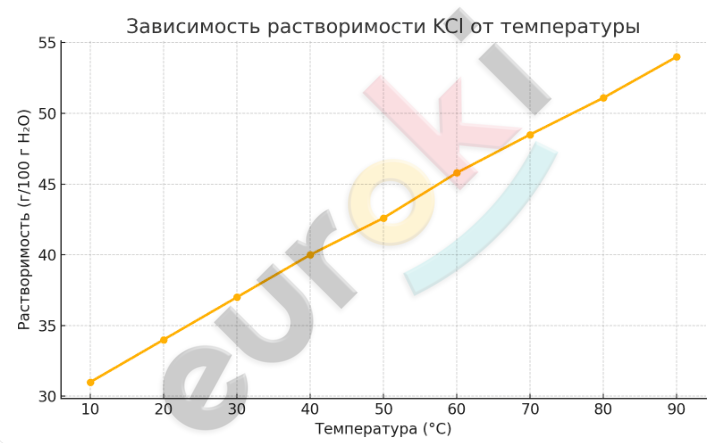
Вывод по графику
Растворимость хлорида калия увеличивается с ростом температуры, что подтверждает общее правило: большинство твёрдых веществ лучше растворяются при нагревании.
12. В домашних условиях экспериментально изучите растворимость в воде следующих веществ: соль, сахар, питьевая сода, ванилин, лимонная кислота. Для этого примерно одинаковую массу вещества (например, чайную ложку) попробуйте растворить в определённом объёме воды (например, 1/4 стакана). Сделайте вывод о растворимости исследуемых веществ.
Я провёл эксперимент: взял по одной чайной ложке каждого вещества и пытался растворить в 1/4 стакана тёплой воды (примерно 50 мл). Ниже — мои наблюдения:
| Вещество | Растворимость в воде (качественная оценка) | Наблюдения |
|---|---|---|
| Соль (NaCl) | Хорошо растворима | Растворяется полностью за 10–15 секунд, без осадка |
| Сахар (C₁₂H₂₂O₁₁) | Очень хорошо растворим | Полностью исчезает, раствор становится сладким |
| Пищевая сода (NaHCO₃) | Хорошо растворима | Быстро растворяется, немного вспенивается |
| Ванилин | Плохо растворим | Растворяется частично, остаётся осадок |
| Лимонная кислота (C₆H₈O₇) | Отлично растворима | Быстро растворяется, раствор становится кислым |
Вывод:
В ходе эксперимента я установил, что лимонная кислота, сахар, соль и сода хорошо растворяются в воде. Особенно быстро растворились сахар и лимонная кислота. Ванилин растворяется хуже всего — часть осталась на дне. Следовательно, вещества отличаются по растворимости, и это можно легко проверить дома простым опытом.
Параграф 2. Классификация химических реакций
Стр. 12
Вопрос
Химические вещества взаимодействуют друг с другом. Как разобраться в огромном многообразии химических превращений? Какие признаки лежат в основе классификации химических реакций?
Чтобы разобраться в большом многообразии химических превращений, учёные разработали систему классификации химических реакций. Она помогает упорядочить знания и понять, к какому типу относится конкретная реакция, предсказать её ход и продукты.
В основе классификации лежат следующие признаки:
По числу и составу реагентов и продуктов реакции (реакции соединения, разложения, замещения, обмена).
По тепловому эффекту — выделяется ли тепло или поглощается (экзотермические и эндотермические реакции).
По агрегатному состоянию реагентов и продуктов — гомогенные (одна фаза) и гетерогенные (разные фазы) реакции.
По обратимости — обратимые и необратимые реакции.
По наличию катализатора — каталитические и некаталитические реакции.
По изменению степени окисления — окислительно-восстановительные и неОВР.
Такая систематизация позволяет проще ориентироваться в химии, проводить опыты и понимать, какие процессы происходят между веществами.






