Параграф 61 Физика 9 класс Пёрышкин | Конспект
Состав атомного ядра. Ядерные силы
Состав атомного ядра
Открытие нейтрона позволило лучше понять структуру атомных ядер. В 1932 году, одновременно с открытием нейтрона, физики Дмитрий Иваненко и Вернер Гейзенберг предложили протонно-нейтронную модель ядра. В соответствии с этой моделью, любое атомное ядро состоит из двух видов частиц — протонов и нейтронов. Эти частицы получили общее название "нуклоны". Экспериментальные исследования подтвердили справедливость данной модели, что помогло объяснить множество ядерных явлений.
Массовое число и зарядовое число
Общее число нуклонов в ядре называется массовым числом и обозначается буквой A. Массовое число численно равно массе ядра, выраженной в атомных единицах массы, округленной до целых чисел. Зарядовое число (число протонов) в ядре обозначается буквой Z. Оно указывает на положение элемента в периодической системе Менделеева и равно количеству положительно заряженных протонов. Число нейтронов обозначается разностью A−Z.
Изотопы
Изотопы — это атомы одного и того же химического элемента, отличающиеся массой атомного ядра. Изотопы имеют одинаковое количество протонов, но различное число нейтронов. Так, у водорода существует три изотопа: протий 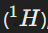 , дейтерий
, дейтерий 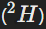 и тритий
и тритий 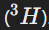 . Каждый из них имеет один протон, но количество нейтронов увеличивается от 0 до 2. Это объясняет различие в массе этих изотопов.
. Каждый из них имеет один протон, но количество нейтронов увеличивается от 0 до 2. Это объясняет различие в массе этих изотопов.
Ядерные силы
Для объяснения устойчивости атомных ядер была выдвинута гипотеза о существовании ядерных сил. Ядерные силы действуют между всеми нуклонами в ядре и значительно превышают по величине электрические силы отталкивания между протонами. Ядерные силы являются короткодействующими: они эффективны на расстояниях порядка 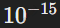 м и не действуют на расстояниях, превышающих
м и не действуют на расстояниях, превышающих 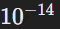 м. Таким образом, эти силы обеспечивают стабильность атомных ядер, преодолевая электростатическое отталкивание между заряженными частицами.
м. Таким образом, эти силы обеспечивают стабильность атомных ядер, преодолевая электростатическое отталкивание между заряженными частицами.