Решебник по химии 9 класс Габриелян | Страница 109
Страница 109
Проверьте свои знания
1. Дайте характеристику элемента углерода на основании его положения в Периодической системе Д. И. Менделеева.
Углерод находится во II периоде, IV A-группе (14 группе) Периодической системы. Его атомный номер 6, следовательно, он имеет 6 протонов и 6 электронов, которые распределяются по электронным уровням: 1s² 2s² 2p². На внешнем энергетическом уровне углерода — четыре электрона, что позволяет ему проявлять валентность IV. Углерод — неметалл, с относительно небольшой атомной массой (12), способен образовывать как ковалентные, так и донорно-акцепторные связи, участвует в образовании органических и неорганических соединений. Химическая активность углерода проявляется как в окислительно-восстановительных реакциях, так и в кислотно-основных взаимодействиях.
2. Сравните свойства алмаза и графита.
Алмаз и графит — это две аллотропные модификации углерода, имеющие разные кристаллические решётки, что определяет их физические свойства. В алмазе каждый атом углерода связан с четырьмя другими атомами прочными ковалентными связями, образуя прочную трёхмерную структуру. Благодаря этому алмаз — самое твёрдое природное вещество, он прозрачен и обладает высоким показателем преломления. Используется в ювелирном деле и в промышленности (резцы, сверла).
Графит состоит из слоёв, в которых атомы углерода связаны в плоскости прочными связями, а между слоями связи слабые, благодаря чему графит мягкий и жирный на ощупь, хорошо проводит ток и тепло. Он используется как смазка, в производстве карандашей, электродов и в ядерной промышленности.
3. Что представляет собой аморфный углерод? Какие виды такого углерода различают? Где их применяют?
Аморфный углерод — это форма углерода, в которой атомы не упорядочены в кристаллическую решётку. В отличие от алмаза и графита, аморфный углерод не имеет строгой структуры. К аморфным формам относят сажу, древесный уголь, активированный уголь, технический углерод и др. Такие формы широко используются: сажа — в производстве красок и резины, активированный уголь — в фильтрах и медицине, древесный уголь — как топливо и в металлургии.
4. Что такое адсорбция? Расскажите о применении этого явления (на примере активированного угля).
Адсорбция — это поглощение веществ из газа или раствора поверхностным слоем твёрдого тела (адсорбента). Вещества, которые оседают на поверхности, называются адсорбатами. Активированный уголь обладает высокой удельной поверхностью и пористостью, благодаря чему способен поглощать газы, пары и растворённые вещества. Он применяется для очистки питьевой воды, в противогазах, в медицине при отравлениях и для очистки растворов в химической промышленности.
5. Охарактеризуйте химические свойства углерода. Ответ подтвердите уравнениями соответствующих реакций.
Углерод проявляет как восстановительные, так и окислительные свойства. Восстановительные свойства проявляются, например, в реакции с оксидами металлов:
(C + ZnO → CO↑ + Zn)
или
(C + CuO → CO↑ + Cu)
Окислительные свойства углерода проявляются в реакциях с металлами при нагревании, например:
(4Al + 3C → Al₄C₃)
или
(Si + C → SiC)
Кроме того, углерод может взаимодействовать с водородом:
(C + 2H₂ → CH₄)
6. Какой процесс называют коксованием каменного угля? Назовите продукты коксохимического производства.
Коксование каменного угля — это процесс термической переработки угля без доступа воздуха при высокой температуре. В результате получается твёрдый пористый углеродистый продукт — кокс, а также образуются побочные продукты: каменноугольная смола, аммиачная вода и коксовый газ. Кокс используют в металлургии как восстановитель, а побочные продукты — в химической промышленности для получения различных органических и неорганических веществ.
Стр. 109
Примените свои знания
7. Используя метод электронного баланса, определите коэффициенты в схеме реакции: (C + HNO₃ → CO₂ + NO₂ + H₂O).
Для составления уравнения реакции с помощью метода электронного баланса необходимо выполнить следующие шаги:
Определим окислительные и восстановительные реакции. Углерод (C) в данной реакции окисляется, так как его степень окисления меняется с 0 до +4 (в CO₂).
Азот в азотной кислоте (HNO₃) имеет степень окисления +5. После реакции азот окисляется до +4 (в NO₂), что свидетельствует о его восстановлении.
Теперь составим полное уравнение с учетом электронного баланса:
(C + 4HNO₃ → CO₂ + 2NO₂ + 2H₂O).
8. Напишите уравнение реакции углерода с оксидом меди(II), серой, оксидом свинца(IV), магнием. Определите, какие свойства — окислительные или восстановительные — проявляет углерод в каждой из реакций.
Углерод с оксидом меди(II) (CuO):
(C + CuO → CO₂ + С )
В этой реакции углерод восстанавливает медь, проявляя восстановительные свойства.
Углерод с серой (SO₂):
(C + SO₂ → CO₂ + S)
В этой реакции углерод окисляется, проявляя окислительные свойства.
Углерод с оксидом свинца(IV) (PbO₂):
(C + PbO₂ → CO₂ + PbO)
Углерод восстанавливает свинец, проявляя восстановительные свойства.
Углерод с магнием (MgO):
(C + MgO → CO₂ + Mg)
Углерод восстанавливает магний, проявляя восстановительные свойства.
9. Какая масса кокса (условно чистый углерод) потребуется для получения цинка из 216 г рудного концентрата, содержащего 75 % оксида цинка, если кокса необходимо взять в двукратном избытке?
Молекулярная масса оксида цинка (ZnO) равна 81 г/моль.
Из 216 г руды 75% составляет оксид цинка:
(216 г × 0.75 = 162 г ZnO)
Количество вещества ZnO:
(162 г ÷ 81 г/моль = 2 моль ZnO)
Для восстановления цинка необходимо использовать углерод, который восстанавливает ZnO по следующему уравнению:
(ZnO + C → Zn + CO)
На каждый моль ZnO требуется 1 моль углерода. Следовательно, для восстановления 2 моль ZnO потребуется 2 моль углерода.
Масса углерода (кокса), необходимая для реакции, равна:
(2 моль × 12 г/моль = 24 г)
В связи с двукратным избытком кокса, необходимая масса углерода составит:
(24 г × 2 = 48 г)
Ответ: для получения цинка потребуется 48 г кокса.
Стр. 109
Используйте дополнительную информацию
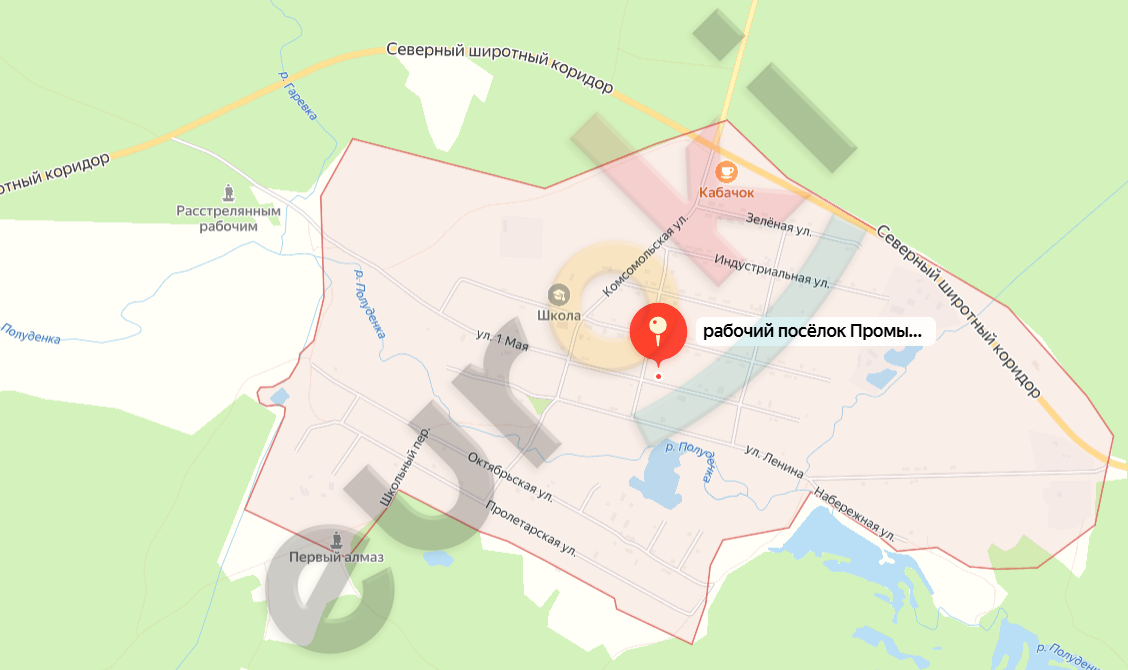
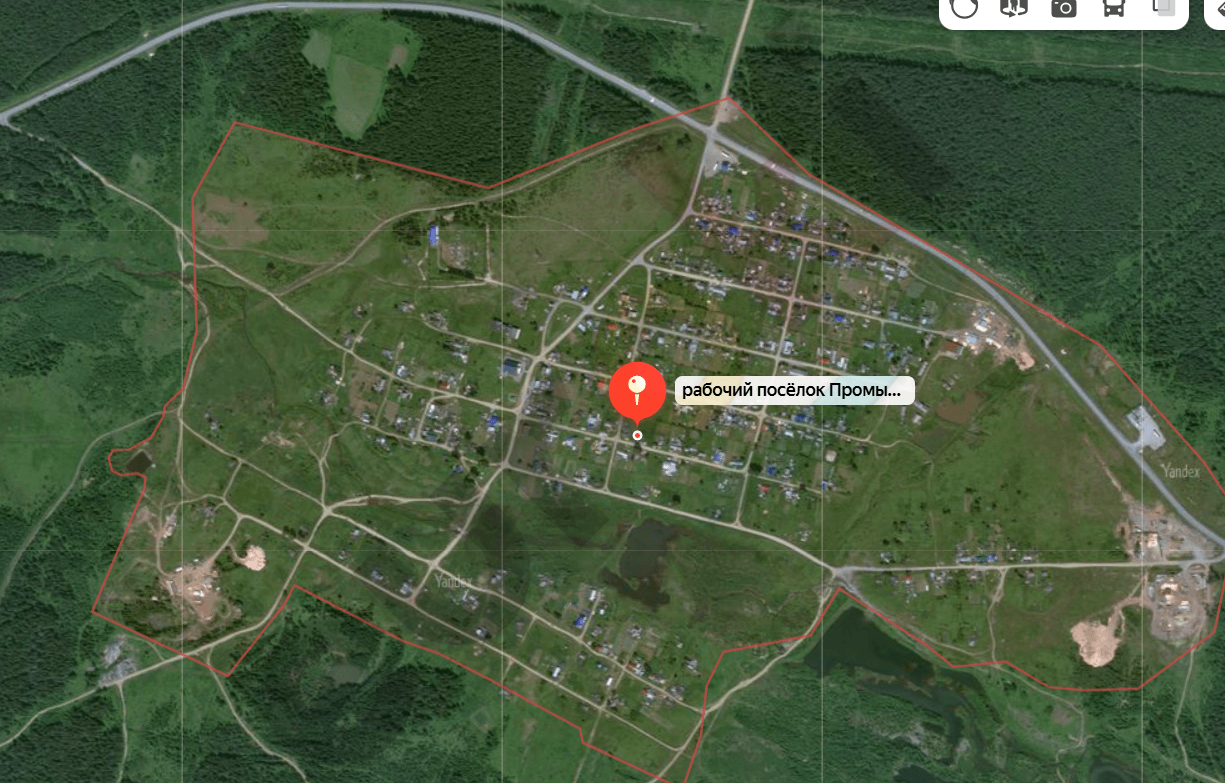
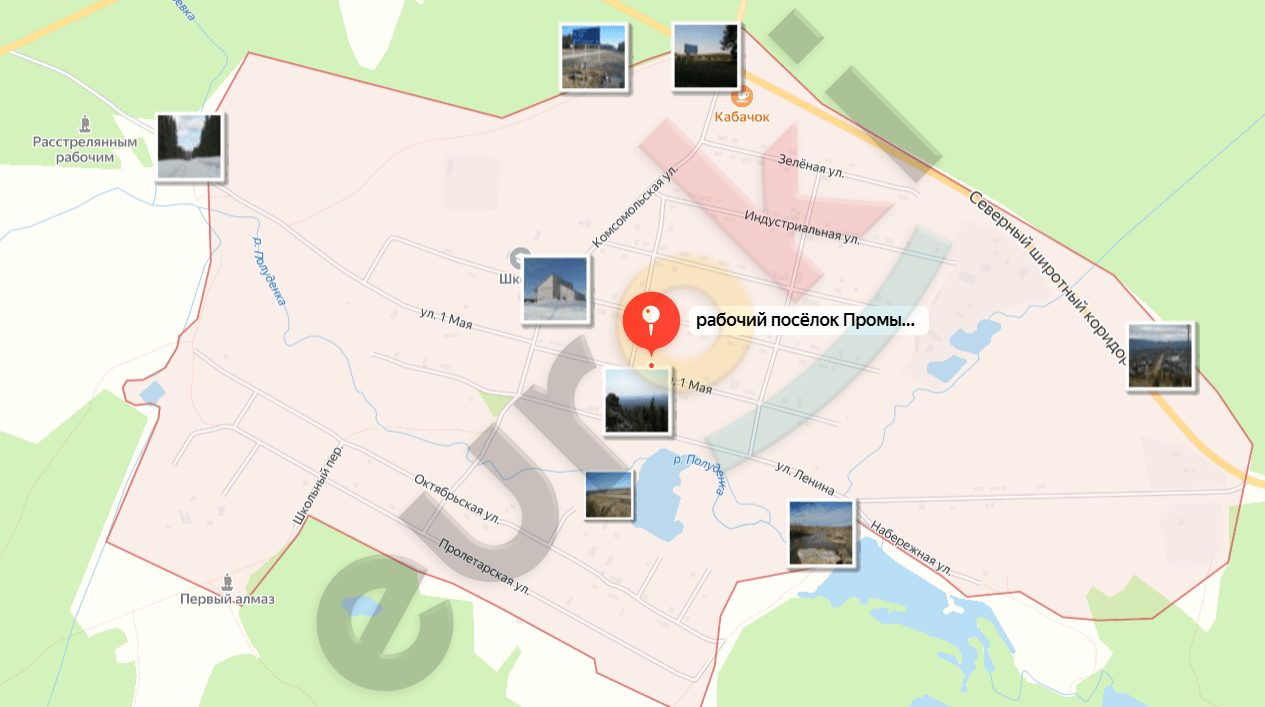
10. Первый в России алмаз был найден 5 июля 1829 г. на Урале в Пермской губернии на Крестовоздвиженском золоторудном прииске четырнадцатилетним крепостным Павлом Поповым. Прииск был расположен недалеко от посёлка Промысла Горнозаводского района Пермского края. Найдите это место на сервисе электронных карт, распечатайте карту и спутниковую съёмку окрестностей посёлка Промысла, определите его географические координаты и расстояние до районного центра Горнозаводска и столицы края Перми.
Его географические координаты: 58,0000° северной широты и 57,5000° восточной долготы. Посёлок Промысла находится в Горнозаводском районе Пермского края России.
Расстояния:
До Горнозаводска: около 30 км на юго-восток.
До Перми: примерно 100 км на северо-восток.
11. Каким образом имя выдающегося русского химика Николая Дмитриевича Зелинского связано с химией углерода? Какое техническое изобретение было сделано им совместно с инженером Эдуардом Куммантом? Подготовьте сообщение о принципе действия и устройстве фильтрующего противогаза.
Николай Дмитриевич Зелинский был выдающимся химиком, чьё имя связано с развитием химии углерода, а также с созданием фильтрующего противогаза. В 1915 году он вместе с инженером Эдуардом Куммантом создал фильтрующий противогаз, который стал важным изобретением в области химической защиты во время Первой мировой войны.
Зелинский и Куммант использовали активированный уголь для фильтрации воздуха от отравляющих химических веществ, таких как хлор и аммиак. Это изобретение обеспечивало солдатам защиту от химических атак, что сыграло ключевую роль в обороне.
Сообщение
Принцип действия и устройство фильтрующего противогаза, изобретенного Н. Д. Зелинским и Э. Куммантом
Николай Дмитриевич Зелинский — один из самых выдающихся русских химиков, чьи исследования значительно повлияли на развитие химической науки и технологий. Его работы охватывали множество аспектов химии, в том числе химию углерода. Именно эта область знаний сыграла ключевую роль в одном из самых важных изобретений Зелинского — фильтрующем противогазе, который стал важным шагом в обеспечении химической защиты во время Первой мировой войны.
Вместе с инженером Эдуардом Куммантом Зелинский разработал фильтрующий противогаз, в котором для защиты от химических атак, таких как отравляющие газы, использовался активированный уголь. Это изобретение стало жизненно важным для солдат, сражавшихся на фронте, где химическое оружие, такое как хлор и аммиак, стало обычным средством нападения. Эти химические вещества являются сильными раздражителями и могут вызывать удушье, ожоги дыхательных путей и даже смерть. Использование фильтрующих противогазов стало единственным эффективным способом защиты от этих опасных веществ.
Принцип действия фильтрующего противогаза основан на использовании активированного угля, который обладает уникальными адсорбционными свойствами. Активированный уголь — это вещество с высокой пористостью, которое может поглощать молекулы различных химических веществ. Когда заражённый воздух проходит через фильтрующий элемент, активированный уголь поглощает вредные вещества, очищая воздух, поступающий в дыхательные пути человека.
В фильтрующем противогазе использовалась именно эта способность угля — его высокое сродство к химическим веществам, которые подлежат адсорбции. Это означает, что уголь задерживает молекулы токсичных веществ на своей поверхности, не позволяя им проникать в дыхательную систему. Этот процесс значительно снижает концентрацию отравляющих веществ, делая воздух безопасным для дыхания.
Однако противогаз не только использовал уголь в качестве фильтрующего элемента. В его конструкции были и другие детали, которые обеспечивали надёжную герметизацию и удобство использования. Важно отметить, что противогаз был разработан не только для защиты солдат от химических атак, но и для удобства использования в условиях войны, когда каждый элемент экипировки должен был быть простым в применении и легко переносимым.
Таким образом, изобретение фильтрующего противогаза Н. Д. Зелинским и Э. Куммантом стало важным достижением в области химической безопасности и сыграло решающую роль в защите солдат от химических атак в годы войны. Сегодня противогазы с использованием активированного угля остаются неотъемлемой частью средств защиты от химического загрязнения и опасных веществ.
12. Подготовьте сообщение об одной из аллотропных модификаций углерода: фуллеренах, графене или углеродных нанотрубках.
Сообщение: «Фуллерены: аллотропная модификация углерода и её уникальные свойства»
Фуллерены — одна из самых необычных и интересных аллотропных форм углерода, открытая в 1985 году. Их структура напоминает сферу, состоящую из атомов углерода, связанных между собой в виде особой полигональной сетки, похожей на конструкцию футбольного мяча. Этот уникальный атомный каркас состоит из пяти- и шестиугольников, что придаёт фуллеренам удивительную прочность и стабильность.
Фуллерены названы в честь архитектора Ричарда Бакминстера Фуллера, создателя геодезических куполов, так как их форма напоминает разработанную им геометрическую модель. Фуллерены могут существовать в различных размерах и формах, включая фуллерен C₆₀ (шестидесятиуглеродный) и C₇₀ (семидесятиуглеродный), хотя существует множество других вариантов.
Одной из главных особенностей фуллеренов является их уникальная химическая стабильность и способность к адсорбции различных молекул. Это открывает широкие возможности для их применения в различных областях науки и технологий, включая медицину, энергетику и электронику. Например, фуллерены могут служить «ловушками» для других молекул, в том числе токсичных веществ, что делает их перспективными в качестве носителей для доставки лекарств в организм человека.
Кроме того, фуллерены обладают удивительными электропроводящими свойствами, которые позволяют использовать их для создания новых материалов для электроники. Например, они могут быть использованы в качестве элементов для разработки сверхпроводников, высокоэффективных аккумуляторов и различных датчиков.
С другой стороны, фуллерены привлекли внимание исследователей благодаря своей способности взаимодействовать с другими молекулами и образовывать сложные структуры. Это делает их интересными для создания новых материалов с уникальными свойствами, таких как фуллереновые нанокомпозиты, которые могут использоваться в различных отраслях.
Таким образом, фуллерены представляют собой не только уникальные молекулы углерода с необычной структурой, но и материалы с уникальными физическими и химическими свойствами, которые открывают новые горизонты в науке и промышленности. На сегодняшний день продолжаются активные исследования, направленные на расширение их применения в различных высокотехнологичных областях, включая медицину, экологию и электронику.
Сообщение: «Графен: уникальная аллотропная модификация углерода и её потенциал»
Графен — это однослойный материал, состоящий из атомов углерода, расположенных в виде двумерной решётки, похожей на соты в пчелиных ульях. Это одна из самых популярных и перспективных аллотропных форм углерода, которая была открыта в 2004 году учёными Андре Геймом и Константином Новосёловым, за что они получили Нобелевскую премию по физике в 2010 году.
Графен обладает уникальными физическими и химическими свойствами. Он обладает исключительной прочностью, которая в 200 раз превышает прочность стали, и при этом является очень лёгким и гибким. Этот материал сочетает в себе несколько важных характеристик: он прозрачный, отлично проводит электричество и тепло и при этом очень прочный. Эти свойства делают графен идеальным материалом для множества современных технологий, от сенсоров и аккумуляторов до дисплеев и прочных материалов.
Графен является отличным проводником как электричества, так и тепла, что открывает множество возможностей для его применения в электронике и энергетике. В частности, его можно использовать для создания новых типов аккумуляторов, которые смогут значительно увеличить ёмкость и скорость зарядки по сравнению с традиционными литий-ионными батареями.
Ещё одно важное свойство графена — его высокая проводимость. Это делает его идеальным материалом для использования в сверхпроводниках, а также для создания компонентов, которые будут работать на значительно более высоких частотах, чем традиционные полупроводники.
Кроме того, благодаря своей двумерной структуре графен имеет невероятно большую поверхность, что позволяет использовать его в качестве носителя для различных молекул, например, для разработки эффективных фильтров, накопителей водорода или для повышения эффективности солнечных батарей.
Графен также проявляет себя как материал с исключительными механическими свойствами. Он не только чрезвычайно прочен, но и обладает высокой гибкостью, что открывает новые горизонты для использования графена в различных отраслях, включая аэрокосмическую промышленность, производство гибких и прочных материалов для мобильных устройств и носимой электроники.
Таким образом, графен является одной из самых многообещающих аллотропных форм углерода, которая обладает удивительными свойствами и большим потенциалом для применения в самых разных областях науки и промышленности. Он уже находит своё применение в разработке новых технологий и материалов и, вероятно, в ближайшем будущем окажет революционное влияние на многие отрасли.
Сообщение: «Нанотрубки углерода: структура и применение»
Углеродные нанотрубки — это молекулы углерода, состоящие из однослойных или многослойных графеновых листов, свернутых в трубочку. Эта уникальная структура придает углеродным нанотрубкам исключительные физико-химические свойства, которые делают их невероятно перспективными для множества применений в различных областях науки и техники.
В зависимости от количества слоёв графена углеродные нанотрубки могут быть однослойными (SWCNT — одностенные углеродные нанотрубки) или многослойными (MWCNT — многостенные углеродные нанотрубки). Однослойные нанотрубки обладают очень высокой проводимостью и механической прочностью, что делает их идеальными для использования в нанокомпозитных материалах и различной электронике.
Углеродные нанотрубки обладают высокой прочностью на растяжение, которая в несколько раз превышает прочность стали, а их механическая жёсткость делает их отличными материалами для создания армированных материалов, которые могут быть использованы в аэрокосмической, автомобильной и других отраслях промышленности. Кроме того, нанотрубки обладают исключительной электрической и тепловой проводимостью, что позволяет использовать их в качестве проводников или для создания высокоэффективных систем охлаждения.
Нанотрубки также находят широкое применение в медицине. Например, они могут использоваться в качестве носителей для доставки лекарств в организм. Благодаря своей форме и способности адсорбировать различные молекулы углеродные нанотрубки могут транспортировать активные вещества непосредственно в клетки, что открывает новые возможности в области лечения и диагностики.
Более того, углеродные нанотрубки активно исследуются как потенциальные материалы для создания новых типов батарей, суперконденсаторов и других накопителей энергии. Это связано с их высокой электропроводностью и большой площадью поверхности, что позволяет повысить ёмкость и эффективность хранения энергии.
Таким образом, углеродные нанотрубки представляют собой один из самых интересных и перспективных материалов современности. Они обладают множеством уникальных свойств, которые открывают новые горизонты для их применения в различных областях, таких как электроника, энергетика, медицина и нанотехнологии.
Стр. 109
Выразите свое мнение
13. Коксохимическое производство относится к взрывоопасным. Как вы думаете, почему?
Коксохимическое производство действительно относится к взрывоопасным. Это связано с несколькими факторами, связанными с технологическими процессами, происходящими на этом производстве.
Во-первых, коксование угля — это процесс, при котором уголь нагревается в отсутствие кислорода, что приводит к выделению различных газов, таких как угарный газ (CO), метан (CH₄), аммиачный газ и другие летучие вещества. Эти газы могут быть крайне взрывоопасными, особенно при высокой температуре и давлении. Небольшие утечки или скопление этих газов в замкнутых пространствах могут привести к взрывам.
Во-вторых, в процессе коксования выделяется коксовый газ, который также является горючим и может вызвать взрыв при неправильном обращении с ним или недостаточной вентиляции. Это приводит к необходимости тщательной работы по обеспечению безопасности на таких предприятиях.
В-третьих, при переработке угля образуются аммиачная вода и аммиак, которые также могут быть взрывоопасными при контакте с определёнными химическими веществами или при несоблюдении необходимых стандартов безопасности.
Таким образом, всё это подтверждает, что коксохимическое производство действительно сопряжено с высоким риском возникновения взрывов, и его безопасность требует строгого контроля на всех этапах производства.
Параграф 21. Кислородные соединения углерода






