Решебник по химии 8 класс. Рудзитис ФГОС §27
§27
Воздух и его состав
Вопросы
1. Вспомните из курса «Окружающий мир» состав воздуха.
Воздух состоит из смеси различных газов. Основные компоненты воздуха:
Азот — около 78 %
Кислород — около 21 %
Углекислый газ — около 0,03 %
Благородные газы (гелий, неон, аргон и др.) — около 1 %
Водяные пары и примеси — в зависимости от условий (непостоянно)
2. Нарисуйте диаграмму, отражающую состав воздуха.
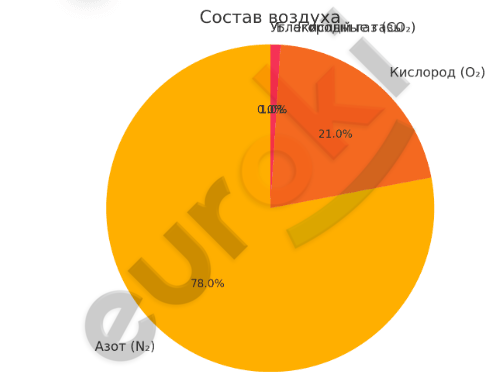
Вот круговая диаграмма, которая отражает состав воздуха:
Азот (N₂) — 78 %
Кислород (O₂) — 21 %
Благородные газы — 1 %
Углекислый газ (CO₂) — 0,03 %
Стр. 96
Подумай, ответь, выполни
1. С помощью каких опытов можно определить содержание кислорода и азота в воздухе?
Содержание кислорода и азота в воздухе можно определить с помощью опыта по сжиганию фосфора под колпаком. При горении фосфор реагирует только с кислородом, в результате чего образуется оксид фосфора. Азот в реакции не участвует. После того как кислород расходуется, уровень воды в сосуде поднимается примерно на 1/5 от объёма, что соответствует объёму кислорода. Таким образом, из опыта можно определить, что воздух состоит примерно из 1/5 кислорода и 4/5 азота по объёму.
2. Какие вы знаете благородные газы? Перечислите области их применения.
К благородным газам относятся: гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe), радон (Rn).
Области применения:
Гелий — заполняют воздушные шары, используют в дыхательных смесях для водолазов, в криогенике.
Неон — применяется в рекламных вывесках, даёт красное свечение.
Аргон — используется для наполнения ламп, при сварке металлов, в научных приборах.
Криптон и ксенон — применяются в источниках света, фарах, лампах-вспышках.
Радон — иногда используется в медицине, но с большой осторожностью из-за радиоактивности.
3. Чем отличается горение веществ в кислороде от их горения на воздухе?
Горение в чистом кислороде происходит значительно быстрее и интенсивнее, чем на воздухе, так как в кислороде отсутствуют инертные газы (например, азот), которые разбавляют кислород. В результате температура пламени выше, пламя ярче и полное сгорание вещества происходит быстрее. На воздухе кислорода лишь около 21 %, и он разбавлен азотом, из-за чего горение идёт медленнее и менее эффективно.
Пример: магний горит в кислороде ослепительно ярким белым пламенем, а на воздухе — тусклее.
4. В чём сходство и различия горения простых и сложных веществ? Поясните на примерах.
Сходство: при горении как простых, так и сложных веществ происходит реакция с кислородом, сопровождающаяся выделением тепла и света. Образуются оксиды.
Различия: при горении простых веществ образуется один продукт — оксид одного элемента, например: (2H₂ + O₂ → 2H₂O) — водород; (C + O₂ → CO₂) — углерод
А при горении сложных веществ (состоящих из нескольких химических элементов) образуются оксиды всех входящих в состав элементов. Например: (2C₂H₂ + 5O₂ → 4CO₂ + 2H₂O) — ацетилен; (C₆H₆ + O₂ → CO₂ + H₂O → уравнивается: 2C₆H₆ + 15O₂ → 12CO₂ + 6H₂O) — бензол
5. Руководствуясь правилами, приведёнными в параграфе, составьте уравнения реакций горения следующих веществ: а) барий; б) алюминий; в) литий; г) фосфор; д) водород; е) сероводород H₂S; ж) этан C₂H₆; з) ацетилен C₂H₂.
а) (2Ba + O₂ → 2BaO)
б) (4Al + 3O₂ → 2Al₂O₃)
в) (4Li + O₂ → 2Li₂O)
г) (4P + 5O₂ → 2P₂O₅)
д) (2H₂ + O₂ → 2H₂O)
е) (2H₂S + 3O₂ → 2SO₂ + 2H₂O)
ж) (2C₂H₆ + 7O₂ → 4CO₂ + 6H₂O)
з) (2C₂H₂ + 5O₂ → 4CO₂ + 2H₂O)
6. Обсудите с соседом по парте условия возникновения и прекращения горения. Какие средства тушения пожара нужно использовать в следующих случаях:
а) загорелась одежда на человеке;
б) воспламенился бензин;
в) возник пожар на складе лесоматериалов;
г) загорелась нефть на поверхности воды?
Условия возникновения горения:
Наличие горючего вещества.
Доступ кислорода (или другого окислителя).
Нагревание до температуры воспламенения.
Прекращение горения возможно при устранении хотя бы одного из этих условий.
Средства тушения пожара:
а) Если загорелась одежда на человеке — накрыть плотной тканью или одеялом, чтобы прекратить доступ воздуха, либо сбить пламя катанием по земле.
б) При воспламенении бензина — использовать пену, песок, углекислотные или порошковые огнетушители, т.к. вода может только растечь бензин.
в) Пожар на складе лесоматериалов — тушить водой, использовать пену или песок, охлаждая материалы и преграждая доступ кислорода.
г) Нефть на воде — использовать пенные огнетушители или специальные вещества, которые создают плёнку на поверхности и перекрывают доступ кислорода. Воду применять нельзя — нефть всплывает.
7. Допишите уравнение реакции горения этана (C₂H₆) в кислороде и расставьте коэффициенты.
Уравнение горения этана: (2C₂H₆ + 7O₂ → 4CO₂ + 6H₂O)
Пояснение:
В этане 2 атома углерода → 2 × 2 = 4 CO₂
6 атомов водорода → 3 H₂O × 2 = 6 H₂O
Всего нужно: 4×2 (O) + 6×1 (O) = 8 + 6 = 14 атомов кислорода → 7 молекул O₂
8. Вычислите объём воздуха, из которого при сжигании было выделено 21 л кислорода. Объёмную долю кислорода округлите до целых.
Объёмная доля кислорода в воздухе ≈ 21 %
Обозначим объём воздуха как V. Тогда:
0.21 × V = 21
V = 21 / 0.21 = 100 л воздуха
9. Вычислите объёмную долю аргона, если из 70 л воздуха выделили 0,63 л аргона.
Обозначим объёмную долю как φ:
φ = (0.63 / 70) × 100 % = 0.009 × 100 = 0.9 %
10. Вычислите объём воздуха, затраченного на получение 100 л кислорода. Объёмную долю кислорода округлите до целых.
Доля кислорода в воздухе ≈ 21 %
Обозначим V — объём воздуха:
0.21 × V = 100
V = 100 / 0.21 ≈ 476.2 ≈ 476 л воздуха
Стр. 97
Тестовые задания
1. Состав воздуха экспериментально определил
1) М. В. Ломоносов
2) А. Лавуазье
3) Дж. Дальтон
4) Дж. Пристли
Правильный ответ: 2) А. Лавуазье
Объяснение: Французский учёный Антуан Лавуазье в 1774 году доказал, что воздух состоит в основном из кислорода и азота, проведя опыты со сжиганием веществ под колпаком.
2. К благородным газам не относят
гелий
кислород
неон
аргон
Правильный ответ: 2) кислород
Объяснение: К благородным газам относятся гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe), радон (Rn). Кислород — активный неметалл, он участвует во многих химических реакциях, в том числе в горении.
3. К реакциям горения относится реакция
CaCO₃ → CaO + CO₂↑
2Mg + O₂ → 2MgO
2HgO → 2Hg + O₂↑
Правильный ответ: 2) 2Mg + O₂ → 2MgO
Объяснение:
Первая реакция — это разложение карбоната кальция при нагревании.
Вторая реакция — взаимодействие магния с кислородом с образованием оксида — это реакция горения.
Третья реакция — это термическое разложение оксида ртути.
Горение — это окислительно-восстановительная реакция с участием кислорода, сопровождающаяся выделением тепла и света. Именно второй вариант ей соответствует.
Стр. 97
С помощью Интернета
1. Используя дополнительные источники информации, ознакомьтесь с биографией Антуана Лорана Лавуазье.
Антуан Лоран Лавуазье — отец современной химии
Антуан Лоран Лавуазье (Antoine Laurent Lavoisier) родился 26 августа 1743 года в Париже в обеспеченной буржуазной семье. Его отец был адвокатом в парламенте Парижа, и семья стремилась дать сыну блестящее образование. Уже в юности Лавуазье проявил выдающиеся способности к наукам, особенно к естественным, математике и химии.
Первоначально Антуан изучал право и даже получил степень бакалавра права в 1763 году, как того требовала семейная традиция. Однако страсть к науке взяла верх, и он полностью посвятил себя научной деятельности. Он учился у лучших преподавателей того времени и серьёзно увлёкся химией, минералогией, геологией и физикой.
В 1768 году, всего в 25 лет, Лавуазье стал членом Французской академии наук. Он занимался самыми разными областями исследований: работал над проблемами водоснабжения Парижа, разрабатывал системы освещения улиц, проводил геологические экспедиции. Но его основной вклад был в химию, где он совершил настоящую научную революцию.
Одним из важнейших достижений Лавуазье стало опровержение теории флогистона — ошибочного представления о том, что при горении из вещества выделяется особая субстанция (флогистон). Вместо этого он доказал, что горение — это реакция соединения вещества с кислородом, который входит в состав воздуха. Для этого он проводил множество опытов по сжиганию различных веществ в закрытых сосудах и точно измерял массу реагентов и продуктов.
Именно Лавуазье экспериментально определил состав воздуха, показав, что он состоит преимущественно из двух газов — кислорода и азота. Он же дал кислороду его современное название и ввёл в обиход термин "гидроген" — «рождающий воду», то есть водород. Он установил, что вода образуется при соединении водорода с кислородом.
Лавуазье стал одним из первых учёных, кто строго придерживался количественного подхода в химии: он точно взвешивал вещества до и после реакций, что позволило ему сформулировать закон сохранения массы: «Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции».
Кроме того, Лавуазье внёс огромный вклад в создание новой химической номенклатуры — он предложил систематические названия веществ, основанные на их составе и свойствах. Эта система положила начало современной химической терминологии.
Он также занимался изучением дыхания, показав, что оно аналогично медленному горению органических веществ в организме. Его исследования легли в основу будущей биохимии.
К сожалению, несмотря на свои заслуги перед наукой, Лавуазье стал жертвой политических событий. Во время Великой французской революции он был связан с налоговой службой (Фермеры генеральные), которая собирала налоги для королевской власти. Это стало причиной его ареста. В 1794 году, в возрасте 50 лет, Антуан Лавуазье был казнён на гильотине. Один из современников сказал: «Для того, чтобы отрубить голову Лавуазье, понадобилась секунда, но столетие не хватит, чтобы создать подобного ему».
Антуан Лоран Лавуазье навсегда вошёл в историю как основоположник современной химии, учёный, который изменил взгляды человечества на природу веществ и химических процессов. Его работы легли в основу всей дальнейшей химической науки.
2. Найдите в Интернете информацию о парниковом эффекте.
Парниковый эффект: механизм, причины и последствия
Парниковый эффект — это естественный процесс, который делает жизнь на Земле возможной. Благодаря ему наша планета сохраняет тепло, получаемое от Солнца. Без этого явления средняя температура на Земле была бы около −18 °C, и жизнь в её привычной форме была бы невозможна. Однако в последние столетия деятельность человека усилила этот процесс, что привело к глобальному потеплению и изменению климата.
Суть парникового эффекта заключается в следующем. Солнечные лучи проходят сквозь атмосферу и достигают поверхности Земли. Поверхность нагревается и начинает излучать энергию в виде инфракрасного теплового излучения. Однако часть этого тепла не уходит обратно в космос, а задерживается в атмосфере благодаря особым газам, называемым парниковыми. Эти газы поглощают и повторно излучают тепло, не позволяя ему покинуть атмосферу. В результате средняя температура воздуха и поверхности Земли повышается.
К основным парниковым газам относятся водяной пар, углекислый газ (CO₂), метан (CH₄), озон (O₃), оксид азота (N₂O), а также фреоны и другие газы техногенного происхождения. Некоторые из них, такие как водяной пар, естественным образом присутствуют в атмосфере. Но концентрация углекислого газа, метана и оксидов азота увеличилась за последние сто лет из-за сжигания ископаемого топлива, вырубки лесов, промышленного производства и сельского хозяйства.
Основными причинами усиления парникового эффекта являются бурное развитие промышленности и транспорта, широкое использование нефти, угля и природного газа, а также уничтожение лесов, особенно в тропических районах. В результате в атмосферу выбрасываются огромные объёмы CO₂ и других газов, которые накапливаются и задерживают всё больше тепла.
Усиление парникового эффекта имеет серьёзные последствия для климата. Температура на планете повышается, полярные ледники тают, уровень мирового океана поднимается. Изменяются погодные условия: учащаются засухи, ливни, ураганы. Всё это влияет на урожайность, вызывает гибель животных и растений, нарушает привычный образ жизни людей.
Чтобы замедлить изменение климата, необходимо принимать меры: переходить на использование возобновляемых источников энергии — солнца, ветра, воды; сокращать вырубку лесов и, наоборот, высаживать новые деревья; улучшать системы переработки отходов; разрабатывать экологически чистые виды транспорта. Кроме того, важно, чтобы страны сотрудничали друг с другом и соблюдали международные климатические соглашения, такие как Парижское соглашение, целью которого является ограничение роста средней глобальной температуры.
Парниковый эффект — это важнейшее природное явление, но его чрезмерное усиление, вызванное деятельностью человека, представляет серьёзную угрозу. Понимание сути этого процесса — первый шаг к решению глобальных экологических проблем XXI века.
Стр. 98







