Решебник по химии 8 класс Габриелян | Страница 52
Страница 52
Лабораторный опыт 8
Что наблюдается при добавлении фенолфталеина в раствор едкого натра (NaOH)?
При добавлении 1–2 капель фенолфталеина в раствор NaOH раствор приобретает ярко-малиновый цвет. Это связано с тем, что фенолфталеин является кислотно-основным индикатором: в щелочной среде он окрашивается в малиновый цвет, а в кислой среде становится бесцветным.
Что происходит при добавлении раствора серной кислоты (H₂SO₄) в раствор NaOH?
При добавлении раствора H₂SO₄ в раствор NaOH происходит нейтрализация – реакция между кислотой и щелочью, приводящая к образованию соли и воды. По мере добавления кислоты окраска раствора исчезает, так как фенолфталеин становится бесцветным в нейтральной среде.
Какой вывод можно сделать из показаний электронных весов до и после реакции?
Показания весов до реакции и после реакции остаются неизменными. Это подтверждает закон сохранения массы веществ, согласно которому масса реагентов равна массе продуктов реакции. В ходе нейтрализации образуется сульфат натрия (Na₂SO₄) и вода (H₂O), но суммарная масса веществ остаётся неизменной.
Запишите схему реакции нейтрализации между NaOH и H₂SO₄.
Схема реакции нейтрализации:
Щёлочь + Кислота → Соль + Вода
NaOH + H₂SO₄ → Na₂SO₄ + H₂O
При этом уравнение реакции с расставленными коэффициентами выглядит так:
2NaOH + H₂SO₄ → Na₂SO₄ + 2H₂O
Эта реакция является классическим примером кислотно-основного взаимодействия, при котором ионы H⁺ из кислоты соединяются с гидроксид-ионами OH⁻ из щёлочи, образуя молекулы воды.
Стр. 52
Лабораторный опыт 9
Что наблюдается при смешивании раствора сульфата железа (III) Fe₂(SO₄)₃ и раствора едкого натра NaOH?
При смешивании раствора Fe₂(SO₄)₃ с раствором NaOH образуется бурый осадок гидроксида железа (III) Fe(OH)₃. Это происходит потому, что ионы Fe³⁺ взаимодействуют с гидроксид-ионами OH⁻, образуя малорастворимое соединение Fe(OH)₃, которое выпадает в осадок. Раствор при этом мутнеет, и в нём образуются характерные хлопья бурого цвета.
Как изменяются показания весов до и после реакции?
Показания весов до и после реакции остаются неизменными, что подтверждает закон сохранения массы веществ. Несмотря на то, что в ходе реакции образуется нерастворимый осадок Fe(OH)₃, масса всех веществ в системе сохраняется, так как никакие вещества не покидают реакционную систему.
Запишите схему реакции между Fe₂(SO₄)₃ и NaOH.
Схема реакции:
Соль + Щёлочь → Другая соль + Нерастворимое основание (осадок)
Fe₂(SO₄)₃ + NaOH → Na₂SO₄ + Fe(OH)₃↓
Полное уравнение реакции с расставленными коэффициентами:
Fe₂(SO₄)₃ + 6NaOH → 3Na₂SO₄ + 2Fe(OH)₃↓
В результате реакции образуется сульфат натрия (Na₂SO₄), который остаётся в растворе, и гидроксид железа (III) Fe(OH)₃, который выпадает в осадок (↓). Это типичная реакция обмена, где два вещества обмениваются своими ионами.
Стр. 52
Проверьте свои знания
1. Что представляет собой химическое уравнение? Какому основному закону химии оно должно соответствовать?
Химическое уравнение – это условная запись химической реакции с помощью химических формул и математических знаков. В уравнении записывают исходные вещества (реагенты) и продукты реакции, а между ними ставят стрелку, показывающую направление процесса. Запись химического уравнения должна соответствовать закону сохранения массы веществ, открытому Михаилом Ломоносовым и Антуаном Лавуазье. Согласно этому закону, масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции. Это означает, что число атомов каждого химического элемента в левой и правой частях уравнения должно быть одинаковым. Для этого используются коэффициенты, уравнивающие число атомов элементов. Если уравнение составлено правильно, оно отражает количественное соотношение между веществами, участвующими в химической реакции.
2. Какой процесс происходит при взаимодействии фосфора и кислорода? Запишите реакцию между этими веществами.
При взаимодействии фосфора (P) и кислорода (O₂) происходит процесс горения, который является экзотермической реакцией (идёт с выделением тепла и света). В результате образуется фосфорный ангидрид (P₂O₅), который является оксидом фосфора. Этот процесс можно записать в виде химического уравнения:
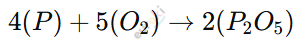
Фосфор сначала соединяется с кислородом, образуя оксид, а затем этот оксид может взаимодействовать с водой, образуя фосфорную кислоту (H₃PO₄). Таким образом, продукт реакции (P₂O₅) является кислотным оксидом, способным вступать в дальнейшие химические взаимодействия.
3. Какую информацию несёт химическое уравнение химической реакции?
Химическое уравнение содержит важную информацию о реакции и её участниках. Оно показывает качественный состав реагентов и продуктов, то есть какие вещества вступают в реакцию и что образуется в результате. Также уравнение отражает количественные соотношения между частицами, позволяя определить число атомов, молекул и моль веществ, участвующих в процессе. Кроме того, химическое уравнение указывает на тип реакции – например, горение, разложение, соединение или замещение. В некоторых случаях в уравнении могут быть обозначены условия реакции (температура, катализаторы, давление). Если уравнение составлено с использованием коэффициентов, оно полностью соответствует закону сохранения массы веществ, что позволяет проводить расчёты по уравнению реакции, предсказывать выход продуктов и определять их массы.







