Решебник по химии 10 класс Габриелян §11
§11
Одноатомные спирты
Стр. 58
Вопрос
1. Химические антонимы «гидратация этилена» и «дегидратация этанола» связывают одно и то же вещество — этиловый спирт C₂H₅OH. Предложите формулу двух гомологов этого соединения, отличающихся от него на группу CH₂. Какую общую формулу имеют спирты этого гомологического ряда и какие свойства для них характерны?
Этиловый спирт имеет формулу C₂H₅OH. Его гомологи — это соединения, отличающиеся друг от друга на одну или несколько групп –CH₂–.
Два ближайших гомолога этанола:
Метанол — CH₃OH
(на одну группу CH₂ меньше)
Пропанол — C₃H₇OH
(на одну группу CH₂ больше)
Общая формула спиртов гомологического ряда: CₙH₂ₙ₊₁OH
Или: CₙH₂ₙ₊₂O
Это формула одноатомных насыщенных спиртов (алканолов).
Характерные свойства спиртов:
-
Физические свойства:
Жидкости или твёрдые вещества (в зависимости от длины цепи).
Хорошо растворяются в воде (особенно низшие спирты).
Имеют характерный запах.
-
Химические свойства:
-
Реагируют с активными металлами (например, натрием), выделяя водород:
(2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂↑)
Образуют сложные эфиры с кислотами (этерификация).
Окисляются до альдегидов, кислот или кетонов.
При нагревании с кислотами могут подвергаться дегидратации с образованием алкенов.
-
Таким образом, спирты представляют собой важный класс органических соединений, обладающих широким спектром химических и физических свойств.
Стр. 60
Вопрос
1. В промышленности этиловый спирт получают в результате реакции гидратации этилена. Какие ещё способы получения спиртов известны?
В промышленности этиловый спирт (C₂H₅OH) получают путём гидратации этилена — присоединения молекулы воды к этилену (C₂H₄) при нагревании и в присутствии катализатора (обычно серной кислоты). Уравнение реакции:
(C₂H₄ + H₂O → C₂H₅OH)
Кроме этого, известны и другие способы получения спиртов:
Гидратация алкенов (в лаборатории):
При взаимодействии алкена с водой в присутствии кислоты в качестве катализатора можно получить спирт.
Например: (CH₂=CH₂ + H₂O → CH₃–CH₂OH)
Замещение в галогенпроизводных алканов:
Галогеналканы можно превратить в спирты путём реакции с раствором щёлочи:
(CH₃–CH₂–Cl + NaOH → CH₃–CH₂–OH + NaCl)
(Это реакция нуклеофильного замещения.)
Брожение сахаров:
В биотехнологии и пищевой промышленности спирты получают путём спиртового брожения глюкозы, при участии дрожжей:
(C₆H₁₂O₆ → 2C₂H₅OH + 2CO₂↑)
Это способ используют для производства алкогольных напитков и пищевого этанола.
Таким образом, спирты можно получать химическим и биотехнологическим путём, и выбор метода зависит от цели, масштабов производства и доступного сырья.
2. Общее свойство органических веществ, характерное и для спиртов, — горение — используют на практике. Какие общие свойства спиртов обусловлены содержанием в их молекуле функциональной гидроксильной группы?
Спирты, как и многие органические вещества, способны гореть. При этом происходит реакция с кислородом, сопровождаемая выделением большого количества тепла и образованиями углекислого газа и воды:
(C₂H₅OH + 3O₂ → 2CO₂ + 3H₂O + Q)
Однако спиртам также присущи особые свойства, связанные с наличием в их молекулах функциональной группы –OH (гидроксильной группы). Эта группа обуславливает следующие общие свойства:
Способность к образованию водородных связей.
Между молекулами спиртов и молекулами воды образуются водородные связи, благодаря которым спирты хорошо растворимы в воде (особенно низшие спирты, например, метанол и этанол).
Полярность молекулы.
Гидроксильная группа делает спирт полярным веществом, из-за чего спирты обладают относительно высокими температурами кипения по сравнению с углеводородами с аналогичной молекулярной массой.
Химическая активность.
Гидроксильная группа легко вступает в реакции, например:
с активными металлами (выделяется водород):
(2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂↑)
с кислотами с образованием сложных эфиров (реакция этерификации):
(CH₃COOH + CH₃OH → CH₃COOCH₃ + H₂O)
с окислителями (окисление до альдегидов или кислот):
(CH₃CH₂OH + CuO → CH₃CHO + Cu + H₂O)
-
Способность проявлять слабые основные и кислотные свойства.
Гидроксильная группа может отдавать или принимать протоны, участвуя в кислотно-основных реакциях.
Таким образом, гидроксильная группа определяет как физические, так и химические свойства спиртов, включая их растворимость, температуру кипения, реакционную способность и способность к образованию водородных связей.
Стр. 61
Лабораторный эксперимент
1. Фильтровальную бумагу положите на керамическую пластинку и нарисуйте на ней шариковой ручкой две точки размером с вишнёвую косточку на расстоянии 5 см друг от друга. В центр первой точки с помощью пипетки нанесите 3—4 капли воды, в центр второй точки — 3—4 капли этилового спирта. Объясните полученный результат.
При нанесении воды на точку на фильтровальной бумаге чернила почти не расплываются, или расплываются очень слабо. Это связано с тем, что вода — полярный растворитель, а большинство чернил в шариковой ручке изготовлены на неполярной или слабополярной основе, и плохо растворимы в воде. Следовательно, вода не разрушает структуру чернил и не разносит их по бумаге.
При нанесении этилового спирта наблюдается расплывание чернил и образование цветного пятна. Этиловый спирт — хороший органический растворитель, он способен растворять чернила, разрушая связи их компонентов, и переносить их по капиллярам фильтровальной бумаги. Это приводит к более сильному и заметному расплыванию пятна.
Таким образом, эксперимент показывает различия в растворяющей способности воды и спирта по отношению к веществам органической природы (в частности, к чернилам), и наглядно демонстрирует, что спирты лучше растворяют органические вещества благодаря своим химическим свойствам.
Стр. 62
Проверьте свои знания
1. Какие вещества относят к классу предельных одноатомных спиртов? Приведите формулы и названия трёх первых представителей этого гомологического ряда.
К классу предельных одноатомных спиртов относятся органические вещества, в молекулах которых углеводородный радикал соединён с одной гидроксильной группой –OH, и которые имеют общую формулу CₙH₂ₙ₊₁OH. Это спирты, образованные от насыщенных (предельных) углеводородов — алканов. Они входят в гомологический ряд, где каждый следующий представитель отличается от предыдущего на одну группу CH₂. Три первых представителя этого ряда:
Метанол (метиловый спирт): CH₃OH
Этанол (этиловый спирт): C₂H₅OH или CH₃CH₂OH
Пропанол (пропиловый спирт): C₃H₇OH, существует в виде двух изомеров — пропанол-1 и пропанол-2.
Эти спирты обладают схожими свойствами: хорошо растворимы в воде, образуют водородные связи, способны гореть, взаимодействуют с активными металлами, кислотами и кислотными остатками с образованием сложных эфиров.
2. Напишите структурные формулы всех спиртов состава C₄H₁₀O, назовите каждое вещество. Укажите типы изомерии, характерные для спиртов. Ответ проиллюстрируйте формулами изомерных бутиловых спиртов.
Молекулярная формула C₄H₁₀O соответствует спиртам с четырьмя атомами углерода и одной гидроксильной группой. Для этого состава возможны структурные и функциональные изомеры:
Бутанол-1 (н-бутиловый спирт): CH₃–CH₂–CH₂–CH₂OH
Бутанол-2 (втор-бутиловый спирт): CH₃–CH₂–CHOH–CH₃
Изобутанол-1 (изобутиловый спирт): CH₃–CH(CH₃)–CH₂OH
Изобутанол-2 (трет-бутиловый спирт): (CH₃)₃C–OH
Эти четыре вещества являются изомерами — у них одинаковый состав, но разное строение. Изомерия спиртов может быть: — структурной (разное положение гидроксильной группы в цепи); — углеродного скелета (разная форма углеродной цепи: прямая или разветвлённая); — функциональной (например, простые эфиры имеют ту же формулу, но другую функциональную группу).
3. Напишите структурные формулы следующих соединений: а) 2-метилпропанол-2; б) 2,3-диметилпентанол-3; в) бутанол-2; г) 3-метилбутанол-2.
а) 2-метилпропанол-2 (трет-бутиловый спирт):
(CH₃)₃C–OH
б) 2,3-диметилпентанол-3:
CH₃–CH(CH₃)–CH(OH)–CH(CH₃)–CH₃
в) бутанол-2:
CH₃–CH₂–CHOH–CH₃
г) 3-метилбутанол-2:
CH₃–CH(CH₃)–CHOH–CH₃
4. Какое действие на организм человека оказывает метиловый спирт? этиловый спирт?
Метиловый спирт (CH₃OH) чрезвычайно токсичен. Его даже небольшое количество может вызвать тяжёлое отравление, повреждение зрения (вплоть до полной слепоты), нарушение работы центральной нервной системы и внутренних органов. В ряде случаев отравление метанолом приводит к смерти. Метанол нельзя употреблять внутрь ни в каком виде.
Этиловый спирт (C₂H₅OH) используется в пищевой, медицинской, косметической и химической промышленности. В умеренных дозах он может вызывать опьяняющее действие, но при регулярном и чрезмерном употреблении вызывает привыкание (алкоголизм), разрушает клетки печени, головного мозга, нарушает работу сердечно-сосудистой и нервной систем. Этанол при передозировке также может привести к тяжёлому отравлению и летальному исходу.
Стр. 63
Примените свои знания
5. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) этан → этилен → этиловый спирт → уксусный альдегид
б) метан → хлорметан → метиловый спирт → метиловый эфир уксусной кислоты
в) этиловый спирт → этилен → бромэтан → этиловый спирт → этанат калия
а) этан → этилен → этиловый спирт → уксусный альдегид
CH₃–CH₃ → CH₂=CH₂ + H₂
CH₂=CH₂ + H₂O → CH₃–CH₂OH
CH₃–CH₂OH + CuO → CH₃–CHO + Cu + H₂O
б) метан → хлорметан → метиловый спирт → метиловый эфир уксусной кислоты
CH₄ + Cl₂ → CH₃Cl + HCl
CH₃Cl + NaOH → CH₃OH + NaCl
CH₃COOH + CH₃OH → CH₃COOCH₃ + H₂O
в) этиловый спирт → этилен → бромэтан → этиловый спирт → этанат калия
CH₃–CH₂OH → CH₂=CH₂ + H₂O
CH₂=CH₂ + HBr → CH₃–CH₂Br
CH₃–CH₂Br + NaOH → CH₃–CH₂OH + NaBr
CH₃–CH₂OH + O₂ → CH₃COOH + H₂O
CH₃COOH + KOH → CH₃COOK + H₂O
6. В двух пробирках без подписей находятся метиловый спирт и толуол. Предложите способ распознавания этих веществ. Напишите уравнение реакции.
Для распознавания можно использовать реакцию с натрием (Na).
Метиловый спирт реагирует с натрием с выделением водорода:
(2CH₃OH + 2Na → 2CH₃ONa + H₂↑) — появляется газ.
Толуол — ароматический углеводород, не реагирует с натрием при обычных условиях. Следовательно, в пробирке, где идёт бурное выделение газа, находится метанол. Где реакции нет — толуол.
7. Какой объём водорода (н. у.) получится при действии 6,9 г натрия на 115 мл этилового спирта плотностью 0,80 г/мл?
Вычислим массу этанола:
m = ρ × V = 0,80 г/мл × 115 мл = 92 г
Найдём количество вещества этанола:
M(C₂H₅OH) = 46 г/моль
n(C₂H₅OH) = 92 / 46 = 2 моль
Уравнение реакции:
(2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂↑)
Из 2 моль этанола и 2 моль натрия выделяется 1 моль H₂.
Найдём количество вещества натрия:
M(Na) = 23 г/моль
n(Na) = 6,9 / 23 = 0,3 моль
Реакция идёт в мольном соотношении 2:1 (Na : H₂), значит:
0,3 моль Na → 0,15 моль H₂
Объём водорода (н. у.):
V = n × Vm = 0,15 × 22,4 = 3,36 л
Ответ: объём водорода, который выделится, равен 3,36 литра.
Стр. 63
Выразите свое мнение
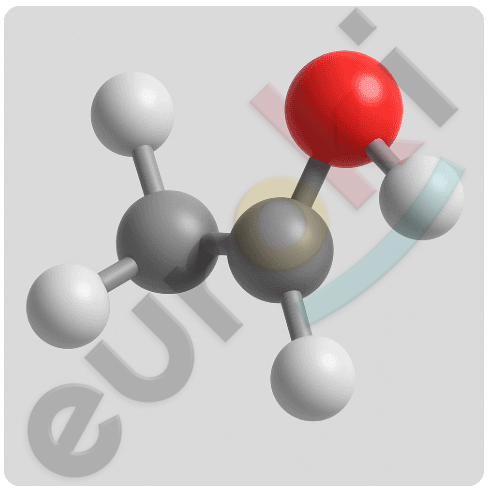
8. Постройте на компьютере 3D-модель молекулы этилового спирта. Рассмотрите взаимное расположение атомов в пространстве. Выскажите и аргументируйте своё мнение о том, является ли расположение атомов C—O—H линейным. Если нет, то определите примерную величину угла.
В молекуле этилового спирта (CH₃–CH₂–OH) атом кислорода связан с атомом углерода и атомом водорода, а также имеет две неподелённые пары электронов. Это придаёт ему изгиб в пространстве, поскольку форма молекулы определяется не только положением атомов, но и электронными парами.
Расположение атомов C—O—H не является линейным, потому что электронные пары кислорода отталкиваются друг от друга и от атомов, образующих связи. Такая геометрия называется изогнутой (или угловой), аналогично молекуле воды.
Примерная величина угла C—O—H составляет около 104–110°, обычно близка к 108°, что подтверждается как экспериментальными данными, так и компьютерным моделированием.
Таким образом, в 3D-модели этанола видно, что угол между атомами C—O—H меньше 180°, и конфигурация не является линейной из-за влияния неподелённых электронных пар кислорода.