Аминокислоты | Конспект
Аминокислоты – это органические амфотерные соединения.
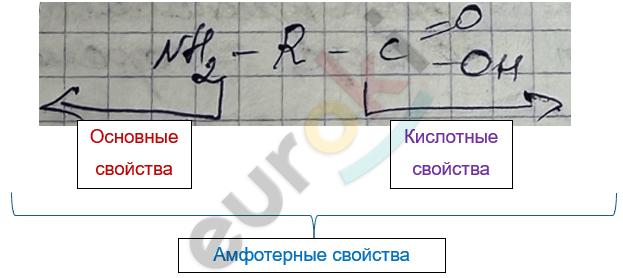
pH = 7
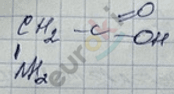
глицин
2-аминоэтановая
2-аминоуксусная
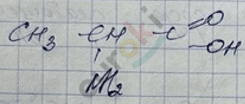
аланин
2-аминопропановая
2-аминопропионовая
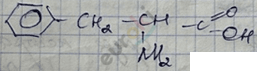
фенилаланин
2-амино-3-фенилпроапновая кислота
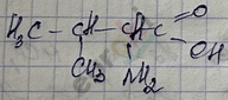
валин
2-амино-3-метилбутановая кислота
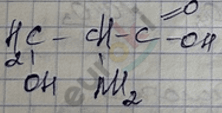
серин
2-амино-3-гидроксипропановая кислота
Физические свойства
Это кристаллические вещества, сладковатые на вкус, хорошо растворимы в воде.
Химические свойства
1. Все реакции по 
Подтверждением кислотных свойств является реакция со щелочами.
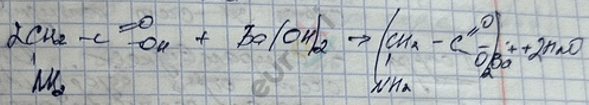
2. Все реакции по \({- \text{NH}}_{2}\) группе как у первичного амина.
Подтверждением основных свойств является реакция с кислотами.

3.
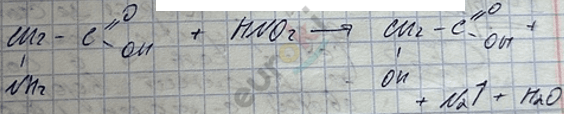
4. Реакция образования пептидов.
а) реакция дегидратации с получением пептидов с числом аминокислот в составе от 2 до 10
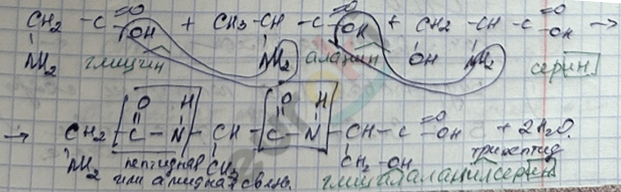
б) реакция поликонденсации в случае образования белка.
Белок (строение)
I структура – это определённая последовательность аминокислот в полипептидной цепи. Образуется за счёт пептидных связей.
II структура – спиралевидная. Образуется за счёт образования водородных связей между пептидными связями витка.
III структура – глобула. Образуется за счёт дисульфидных мостиков (если есть S в составе) и дополнительных водородных связей с молекулами воды.
IV структура
Качественные реакции на белок
1) Биуретовая (на пептидные связи)
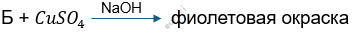
2) Ксантопротеиновая реакция (на бензолсодержащие белки)
Б + \(\text{HNO}_{3}\) (конц.) → жёлтое окрашивание
3) Сульфгидрильная реакция (на S-содержащие белки)
Б + \(\text{Pb}^{2 +}\)→ чёрное окрашивание (PbS↓)
Реакции гидролиза пептидов
1) Водный

2) Кислотный
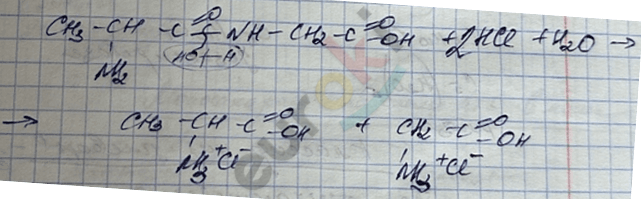
3) Щелочной
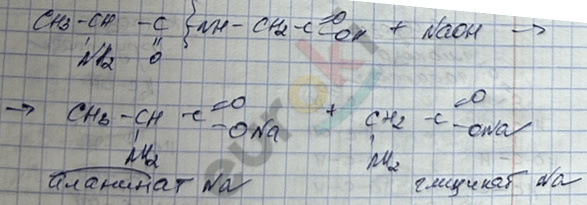
Получение аминокислот
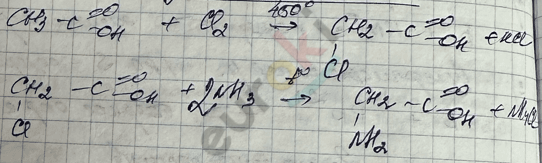
Любые N-содержащие соединения сгорают с получением \(\text{CO}_{2}\), \(H_{2}O\), \(N_{2}\).