Молекулярно-кинетическая теория (МКТ) | Конспект
Все тела состоят из какого-то вещества, и все вещества состоят из молекул.
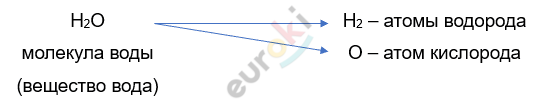
Все молекулы в любом агрегатном состоянии вещества находятся в постоянном хаотичном движении – тепловом движении.
Движение молекул прекращается при достижении температуры абсолютного нуля.
–273°С = 0 К (Кельвин)
27°С = 27° + 273° = 300° К
Температура тела характеризует скорость движения его молекул: чем выше температура, тем быстрее движутся молекулы.
В международной системе единиц количество вещества выражают в молях и считают, что один моль – это количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в углероде массой:
m = 0,012 кг
v («ню») = \(\frac{m}{M}\) = \(\frac{N}{N_{A}}\)
v («ню») – количество вещества (моль)
m – масса вещества (кг)
M – молярная масса
N – количество молекул
\(N_{A}\) = 6,022 · \(10^{23}\) \({моль}^{- 1}\)
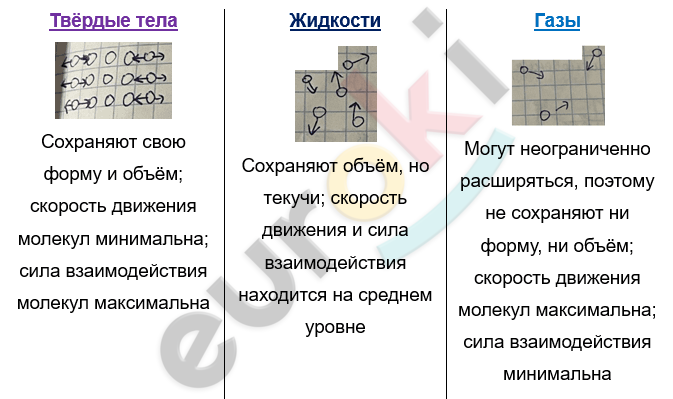
В МКТ рассматривается не реальный газ, а его модель – идеальный газ.
Идеальный газ – это теоретическая модель газа, в которой не учитываются размеры молекул (они считаются материальными точками) и их взаимодействие между собой (за исключением случаев непосредственного столкновения).
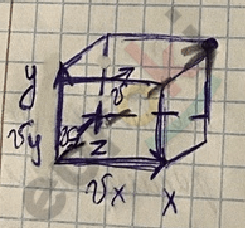
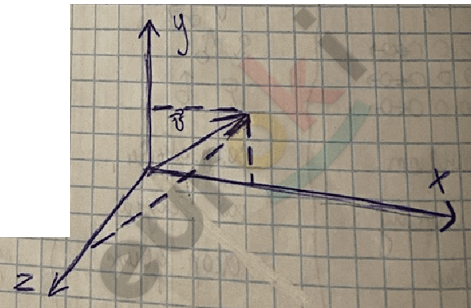
\({\overline{V}}^{2}\) = \({\overline{V}}_{x}^{2}\) + \({\overline{V}}_{y}^{2}\) + \({\overline{V}}_{z}^{2}\)
Квадрат скорости находится на диагонали куба.
\({\overline{V}}^{2}\) = 3\({\overline{V}}_{x}^{2}\)
\({\overline{V}}_{x}^{2}\) = \(\frac{1}{3}\) \({\overline{V}}^{2}\) – средний квадрат проекции скорости (постоянная величина)
P = \(\frac{F}{S}\) = \(\frac{1}{3}\) n\(m_{0}{\overline{V}}^{2}\) – формула связи давления и среднего квадрата скорости
n – количество молекул
m – масса одной молекулы
\({\overline{V}}^{2}\) – средний квадрат скорости
P = \(\frac{2}{3}\) n\({\overline{E}}_{k}\) – связь давления и средней кинетической энергии движения молекул